 |
 |

Effet de l’Activité Physique sur la Fonction Cognitive chez l’Adulte Agé à risque de Maladie d’Alzheimer.Un essai randomisé
Nicola T. Lautenschlager, MD;
Kay L. Cox, PhD;
Leon Flicker, MBBS, PhD;
Frank M. van Bockxmeer, PhD;
Jianguo Xiao, MD, PhD;
Kathryn R. Greenop, PhD;
Osvaldo P. Almeida, MD, PhD
JAMA. 2008;300(9):1027-1037
RÉSUMÉ
 |  |
Contexte De nombreuses études d’observation ont montré qu’une activité physique réduit le risque de déficit cognitif ; il manque cependant une preuve à partir d’essais randomisés.
Objectif Déterminer si l’activité physique réduit le taux de déficit cognitif parmi les adultes âgés à risque.
Conception et Environnement Essai contrôlé randomisé d’intervention de 24 semaines d’activité physique dirigée entre 2004 et 2007 dans la métropole de Perth, Australie Occidentale. Les assesseurs à la fonction cognitive n’étaient pas informés de leur adhésion au groupe.
Participants Nous avons recruté des volontaires qui disaient avoir des problèmes de mémoire mais qui ne répondaient pas aux critères de démence. Trois cent onze sujets de 50 ans et plus ont été examinés pour participer, 89 n’ont pas été sélectionnés, et 52 ont refusé de participer. Un total de 170 participants était randomisé et 138 participants ont terminé l’évaluation à 18 mois.
Intervention Les participants étaient répartis aléatoirement dans un groupe éducatif ou de soin habituel ou dans un programme de 24 semaines d’activité physique à la maison.
Mesure de Résultat Principal Changement dans les scores dans l’échelle permettant la quantification des fonctions cognitives des patients Alzheimer (ADAS-Cog) (variation possible, 0-70) sur 18 mois.
Résultats Dans une analyse en intention de traiter, les participants du groupe d’intervention se sont améliorés de 0,26 points (intervalle de confiance 95%, - 0,89 à 0,54) et ceux du groupe de soin habituel se sont détériorés de 1,04 points (intervalle de confiance 95%, de 0,32 à 1,82) sur l’échelle ADAS-Cog à la fin de l’intervention. La différence absolue de la mesure du résultat entre les groupes d’intervention et le groupe-contrôle était de -1,3 points (intervalle de confiance 95%, de -2,38 à -,22) à la fin de l’intervention. A 18 mois, les participants du groupe d’intervention se sont améliorés de 0,73 points (intervalle de confiance 95%, -1,27 à 0,03) sur ADAS-Cog, et ceux du groupe de soin habituel se sont améliorés de 0,04 points (intervalle de confiance 95%, -0,46 à 0,88). La liste de mots à rappel différé et l’Echelle CDR (Clinical Dementia Rating sum of boxes) qui tient compte à la fois des déficits cognitifs et des activités de la vie quotidienne, s’est améliorée modestement également, alors que la liste totale de mots à rappel immédiat, le test de codage, l’aisance verbale, le score Beck de dépression, et le questionnaire abrégé de 36 questions de l'étude sur les résultats médicaux et les résumés des composants physiques et mentaux n’ont significativement pas changé.
Conclusions Dans cette étude sur des adultes ayant une atteinte subjective de la mémoire, un programme de 6 mois d’activité physique a fourni une amélioration modeste de la cognition sur une période de suivi de 18 mois.
Enregistrement de l’Essai anzctr.org.au Identifiant : ACTRN12605000136606
Comme la population mondiale vieillit, on estime que le nombre d’adultes âgés atteints de maladie d’Alzheimer (MA) va augmenter de 26,6 millions actuels à 106,2 millions en 2050.1 Si le début de la maladie pouvait être retardé de 12 mois, il y aurait 9,2 millions de cas en moins dans le monde. 1 Pour cette raison, des tentatives ont été faites pour identifier les sujets qui présentent un risque de MA et pour tester des interventions qui pourraient retarder la progression de symptômes prodromaux vers la démence totale. Les résultats d’études d’observation suggèrent que les personnes âgées exemptes de démence mais qui rapportent une baisse de mémoire ou montrent une évidence objective d’atteinte cognitive ont plus de chances de développer une MA dans le temps. 2,3
Sept essais cliniques ont examiné si les inhibiteurs de la cholinestérase (donepezil, rivastigmine et galantamine), la vitamine E, le piracetam et le rofecoxib (inhibiteur de la cyclooxygénase 2) peuvent prévenir le déficit cognitif et la progression vers la démence chez les adultes âgés avec de légères atteintes cognitives. Dans un essai de Petersen at al., 4 769 participants avec une légère atteinte cognitive ont reçu aléatoirement 10 mg de donepezil, 2000UI de vitamine E ou un placebo quotidiennement pendant 36 mois. A la fin de l’étude, la progression vers la démence et les changements dans les scores cognitifs ne différaient pas selon le groupe de traitement. Une étude de la rivastigmine pour prévenir la conversion de légères atteintes cognitives à la démence sur 4 ans a annoncé de semblables découvertes négatives. 5 Des résultats préliminaires de deux essais à la galantamine 2 qui doivent être encore complétés étaient également négatifs, 6 comme le furent les découvertes des essais sur le piracetam et le rofecoxib. 7 D’autres stratégies pour prévenir le déficit cognitif et la démence chez des personnes à risque sont actuellement testés, mais les résultats disponibles ont été contradictoires pour les vitamines B, 8,9 les statines,10 et la thérapie anti-hypertensive 11,12
De nombreuses études d’observation ont montré que les personnes qui sont actives physiquement semblent être moins sujettes que les personnes sédentaires à développer un déficit cognitif et une démence plus tard dans la vie. Weuve et al13 ont rapporté que des niveaux plus élevés d’activité physique pendant 2 ans pour les 18 766 femmes de l’Etude de Santé des Infirmières étaient associés à des scores cognitifs améliorés. De même, Abbott et al14ont repporté que des hommes qui font au moins 3kms de marche par jour ont 1,8 moins de chances de développer une démence sur une période de suivi de 6 ans. Des études prospectives ultérieures ont confirmé que l’activité physique est associée à une incidence réduite de démence.15,16 et elle a montré que l’association activité physique et fonction cognitive est apparente même lorsque l’exercice est limité, à un âge avancé.17Cependant, il manque toujours une preuve pour le confirmer par des essais randomisés.
Nous avons conçu l’essai randomisé présent pour tester si une intervention d’activité physique à la maison sur 24 semaines réduisait le taux de déficit cognitif chez l’adulte âgé à risque élevé de démence.
METHODES
Participants
L’Etude de la Santé pour le Cerveau Vieillissant (FABS en anglais) fut un essai contrôlé randomisé sur un seul site mené entre Mai 2004 et Janvier 2007 à l’Hôpital Royal de Perth en Australie. Les participants avaient été recrutés entre Mai 2004 et Juillet 2006 de diverses manières, y compris par annonces dans des médias locaux et 2 cliniques de la mémoire.
Des volontaires de 50 ans et plus avaient été examinés par Enquête Téléphonique pour le Statut Cognitif Modifié. Ceux dont les scores étaient inférieurs à 19 sur 50 étaient exclus du fait de l’évidence d’atteinte cognitive significative. 18 De même, les sujets avec un score de 6 ou plus dans l’Echelle 1519 de Dépression Gériatrique étaient exclus de l’étude du fait de la présence de symptômes dépressifs cliniquement significatifs. Etaient aussi exclus ceux dont il était rapporté qu’ils ingéraient plus de 4 unités d’alcool standard par jour ; ceux qui avaient une maladie mentale chronique, comme la schizophrénie ; ou une maladie qui mettait leur vie en danger, comme un cancer métastasé, ou qui les rendaient incapables de s’engager dans une activité physique, comme une insuffisance cardiaque sévère. D’autres critères d’exclusion incluaient une atteinte sensorielle sévère ou un manque d’aisance en anglais écrit ou parlé.
Les participants potentiellement éligibles étaient invités à prendre part à une évaluation personnelle qui comprenait l’Examen Mini Mental State,20la Classification Internationale Statistique des Maladies, 10è Révision (ICD-10 en anglais), l’Evaluation de la Démence Clinique, 21 et la Batterie d’Evaluation neuropsychologique du Consortium pour Etablir un Registre de la Maladie d’Alzheimer.22 Les sujets qui répondaient aux critères de recherche ICD-10pour le diagnostic de démence23 étaient exclus de toute participation ultérieure, comme l’étaient ceux qui avaient un score inférieur à 24 dans l’Examen de Mini Mental State, un score dans l’échelle d’Evaluation de Démence Clinique de 1 ou plus, ou ceux qui étaient incapables de marcher pendant 6 minutes sans aide.
Les volontaires étaient éligibles pour la randomisation s’ils répondaient oui à la question : « Avez-vous des problèmes de mémoire ? » indépendamment du fait qu’ils montraient une preuve de leur trouble cognitif objectif. Les participants étaient considérés comme ayant de légers troubles cognitifs si leur score était de 1,5 SD ou moins que la moyenne des scores du groupe-contrôle de la Batterie Cognitive du Consortium pour Etablir un Registre pour la Maladie d’Alzheimer de leur âge et sexe24dans les sous-tests pour l’aisance verbale, l’attribution d’un nom à un objet représenté en peinture, le rappel immédiat et différé d’une liste d’objets, et la praxie. Il fallait aussi que les participants aient obtenu un accord de leur médecin de famille pour prendre part à une activité physique.
Les comités d’éthique et de recherche humaine de l’Université d’Australie de l’Ouest et de l’Hôpital Royal de Perth ont approuvé cette étude, et tous les participants ont apporté leur consentement éclairé écrit.
Evaluation et Activité Physique
Nous avons utilisé l’enquête du Programme d’Activités pour une Communauté en Santé (CHAMPS en anglais) pour évaluer l’activité physique.25On demandait aux participants de compléter le questionnaire CHAMPS deux fois durant les 2 semaines de sélection ou la période de préparation pour les familiariser avec toutes les questions. Les données du premier questionnaire étaient méconnues, alors que le second fournissait les données pour suivre les mesures du résumé. Les mesures d’activité physique incluaient des minutes par semaine passées à des activités liées à des exercices, des minutes par semaine passées sur toutes les activités modérées et plus, et les calories dépensées dans toutes les activités modérées et plus. Les activités modérées et plus comprenaient des activités d’intensité modérée, importante et très importante (ex marche rapide, danse de salon, gym en circuit training, ou natation). De plus, tous les participants portaient un podomètre (Digi-Walker SW-700, Yamax Inc, Tokyo, Japon) pendant l’évaluation des 7 jours de base avec les CHAMPS, aussi bien que durant la semaine précédant les évaluations sur 6-, 12-, et 18 mois. Ceci a fourni une mesure objective et valable, résumée en un nombre total de pas effectués en une journée.26Les participants notaient cette information dans un journal, dans lequel étaient également notés les moments où le podomètre était en fonction ou non. Lorsque les participants réalisaient des activités sans faire de pas (comme nager ou faire du vélo), l’intensité de l’activité était décidée et le nombre équivalent de pas estimé et ajouté à l’enregistrement quotidien, comme l’ont souligné Miller et al.27Comme 10 000 pas par jour sont associés à des résultats d’amélioration de l’état de santé, 28 les participants avec un compte de pas par semaine plus grand ou égal à 70 000 étaient classés comme actifs et le restant, comme non actifs.
Evaluation de la Fonction Cognitive, Dépression et Qualité de Vie
L’échelle d'évaluation des fonctions cognitives des patients Alzheimer (ADAS-Cog en américain) fut la mesure primaire du résultat de l’étude.29L’échelle consiste en 11 tests cognitifs brefs évaluant la mémoire, le langage, et la praxie. Les scores vont de 0 à 70, avec les scores les plus élevés indiquant une sévérité plus importante ou un trouble cognitif. Les mesures cognitives d’intérêt secondaire comprenaient (1) le nombre de mots rappelés avec délai (de 0 à 10) et sans (de 0 à 30) de la Batterie d’Evaluation neuropsychologique du Consortium pour Etablir un Registre de la Maladie d’Alzheimer, (2) le score total dans le Test de Codage (scores possibles, 0-133),30 et (3) l’aisance verbale (nombres de mots commençant par F, A, et S que l’individu peut dire en une minute) selon la mesure de la Batterie de Tests Delis-Kaplin Fonction Executive.31 Tout au long de l’essai, nous avons contrôlé la fréquence et la sévérité des symptômes dépressifs avec l’Inventaire Beck de la Dépression (de 0 à 63, avec des scores plus élevés indiquant de plus grands niveaux de symptômes dépressifs),33 et la qualité de vie avec le questionnaire abrégé de 36 questions de l'étude sur les résultats médicaux et les résumés des composants physiques (SF-36) (tous deux avaient une norme de population de 150 points, avec des scores plus bas indiquant une piètre qualité de vie).34
Génotype Apolipoprotéine
Nous avons déterminé le génotype apolipoprotéine (APOE) en utilisant les procédures standard décrites auparavant. 35
Randomisation
A la fin de l’évaluation de la ligne de base, les participants étaient répartis au hasard dans un programme d’activité physique ou un contrôle de soin habituel selon une liste de nombres aléatoires générée par ordinateur par séries de 8 (4 personnes réparties aléatoirement dans chaque groupe). Les nombres de répartition étaient conservés dans des contenants scellés et étaient tirés par un chercheur qui n’était pas directement impliqué dans le recrutement ou l’évaluation de participants. En raison de la nature de l’intervention, les participants étaient informés de leur appartenance au groupe, mais le personnel de recherche entreprenant les évaluations cognitives n’était pas informé. Pour assurer la conformité aux procédures, le personnel de recherche qui dirigeait l’intervention d’activité physique étaient hébergé dans un bâtiment différent et étaient soumis à une surveillance indépendante. On demandait explicitement aux participants au début de l’essai et lors de chaque évaluation suivante de ne pas divulguer d’information concernant l’intervention avec le personnel de recherche dirigeant l’évaluation de la fonction cognitive. De même, des instructions avaient été données au personnel de recherche dirigeant l’évaluation cognitive de ne pas parler avec les participants des aspects de l’intervention. Le personnel de recherche d’activité physique et d’évaluation cognitive était surveillé par divers enquêteurs de l’équipe FAB. Nous n’avons pas été informés de quelque faille que ce fût pendant le déroulement de l’essai.
Groupe témoin soins habituels
Les participants de ce groupe ont reçu du matériel pédagogique sur la perte de mémoire, la gestion du stress, le régime alimentaire sain, la consommation d’alcool, et de cigarette mais pas sur l’activité physique. On a offert au groupe d’activité physique ces matériaux pédagogiques.
Intervention d’Activité Physique
Le but de l’intervention était d’encourager les participants à avoir au moins 150 minutes d’activité physique d’intensité modérée par semaine,36que les participants devaient réaliser en trois sessions de 50 minutes chacune chaque semaine. Le régime de 3 sessions par semaine a été sélectionné parce que des expériences antérieures avaient montré que ce rythme était acceptable pour les participants et parce que c’était plus pratique logistiquement et financièrement pour ceux qui avaient choisi des activités qui nécessitaient de venir assister à des classes ou d’aller en centre.36 Ceux qui étaient déjà en train de terminer le but fixé à la ligne de base étaient encouragés à ajouter une autre session de 50 minutes par semaine (1 session) à leur niveau d’activité individuel. Le programme personnalisé d’activité physique à la maison et le manuel pour l’ensemble de l’intervention comportementale était donné pendant un entretien de 60 minutes avec un membre du personnel formé à l’activité physique. Le type d’activité le plus fréquemment recommandé était la marche. Cependant, les participants pouvaient choisir d’autres formes d’exercices pour terminer les 3 sessions de 50 minutes par semaine. Douze participants choisirent d’inclure dans leur programme quelques exercices d’entraînement de force légère. Ceux-ci étaient ceux qui étaient déjà actifs et avaient eu une expérience antérieure d’exercice de gymnastique en circuit training. A part 1 participant, tous choisirent la marche ou d’autres exercices d’aérobic aussi bien que des activités d’entraînement de force. Puis les participants reçurent des bulletins par courrier semaine 2, 8, 14, 20, 32, 4à 65 et 72 pour renforcer les messages-clés du programme. L’intervention ne comprenait pas d’équipement à la maison.
On demandait à tous les participants d’utiliser un journal simplifié pour enregistrer leur activité physique et de renvoyer leur journal au surveillant chaque mois par retour prépayé. L’adhésion était calculée à partir du nombre de journaux mensuels enregistré et était défini comme étant le pourcentage d’activité physique terminée comparé au total d’activité physique prescrit.
Intervention Comportementaliste
Pour augmenter l’adhésion au programme, les participants reçurent également un ensemble d’intervention comportementale modifié basé sur la théorie sociale cognitive.37 L’ensemble était livré par le biais d’atelier, de manuel, de bulletins et d’appels téléphoniques. Le manuel et les bulletins contenaient une information sur les programmes d’exercices, les récompenses, l’établissement de buts, la gestion du temps, les limites aux activités, et un exercice sûr. Pendant l’intervention de 24 heures, les participants ont été soumis à un entretien structuré par téléphone pour contrôler les progrès du programme d’activité physique et pour encourager la conformité continue. (Le protocole original spécifiait que 6 appels téléphoniques seraient faits pendant l’intervention, mais en raison de moyens limités et la nécessité d’essayer de joindre les participants plusieurs fois avant de réussir à les avoir, le nombre moyen d’appels a été diminué à [SD] 2,0 [1,1], et chaque appel durait en moyenne 10,5 [9,0] minutes.)
Visites de Suivi
Nous avons répété l’évaluation de l’activité physique, de la fonction cognitive, de l’humeur, et de la qualité de vie à 6, 12 et 18 mois après la ligne de base. Les participants dans l’intervention d’activité physique étaient encouragés à rester physiquement actifs, sans aucune intervention ultérieure autre que 4 bulletins, décrits plus haut.
Calcul de Puissance
Nous avons rassemblé des données prospectives ADAS-Cog sur 12 mois à partir d’un échantillon indépendant d’adultes âgés avec des plaintes subjectives au sujet de leur mémoire, vivant à Perth. Les résultats montraient un écart type augmenté (SD) de 3,5 (4,5) points pendant cette période. Du fait qu’il était plus probable que les participants soient à risque de troubles plus que ceux de l’échantillon indépendant, nous avons alors estimé que les scores ADAS-Cog de participants ne recevant pas d’intervention d’activité physique se détérioraient de 2,5 points supplémentaires par an (total, 6,0 points ; SD, 4,5). Ceci représente la plus petite différence que l’on considérait comme étant cliniquement significative dans les essais cliniques. 38 La participation de 84 volontaires dans chacun des 2 groupes (n = 168) sur la ligne de base a abouti en une puissance de 90% avec 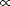 .05. Nous avons estimé un taux d’abandon à 20%, ce qui a conduit à un recrutement de 170 participants avec une puissance de 80% (85 attribués aléatoirement à chaque groupe). .05. Nous avons estimé un taux d’abandon à 20%, ce qui a conduit à un recrutement de 170 participants avec une puissance de 80% (85 attribués aléatoirement à chaque groupe).
Analyse de Données
Les données furent analysées en utilisant SAS pour Windows version 9.1 (SAS Institute Inc, Cary, Caroline du Nord) et SPSS 15.0 pour Windows (SPSS Inc, Chicago, Illinois). Pour des variables continues normalement distribuées, les moyennes arithmétiques et les SD (écarts types) ont été calculés. Pour des variables continues transformées logarithmiquement, les moyennes géométriques et les SD ont été calculés par ordinateur. Pour la comparaison de base de ligne entre les groupes d’exercices et de contrôle de soin usuel, on a utilisé la méthode Pearson dans l’enquête des données catégoriques, le résultat statistique étant distribué selon la loi de  2. Pour des variables distribuées normalement dans l’analyse des caractéristiques de base entre les 2 groupes, des tests t ont été menés. 2. Pour des variables distribuées normalement dans l’analyse des caractéristiques de base entre les 2 groupes, des tests t ont été menés.
Les 3 points de suivi dans le temps ont été établis à 6, 12 et 18 mois. Nous avons utilisé 2 stratégies analytiques différentes pour déterminer les différences entre groupes. L’analyse primaire était basée sur une analyse en intention de traiter en utilisant la procédure d’imputation multiple SAS. Pour les variables positives biaisées, les transformations de logarithmes étaient appliquées avant les imputations. Des scores de base de ligne à 6, 12 et 18 mois ont été inclus dans le modèle d’imputation en plus du sexe, de l’éducation, du QI prémorbide et du statut marital. Nous avons dirigé 5 imputations en utilisant une chaîne d’interactions séquentielles avec un ensemble de 200 interactions suivi de 100 interactions entre les imputations successives. Chaque ensemble de données imputé était analysé en utilisant un modèle des effets mixtes avec des mesures répétées, et on faisait la moyenne des estimations de paramètres parmi les ensembles de données. L’analyse en intention de traiter était alors suivie par une analyse de cas complet, dans laquelle les participants avec des données valables en tous points de temps étaient inclus dans l’analyse.
Une procédure de mesures répétées était utilisée et une analyse de covariance (ANCOVA) dans les analyses à la fois en intention de traiter et de cas complets. Pour les données en intention de traiter un modèle mixte avec des mesures répétées en SAS était utilisé alors que pour des données de cas complet, un modèle général linéaire pour des mesures répétées ANCOVA en SPSS était utilisé. Quatre points de temps étaient traités comme facteur intra-participants (effet sur le temps) et les différences entre l’exercice et le groupe-contrôle de soin habituel étaient traités comme facteur intra-participants. Les interactions entre les facteurs intra-participants et inter-participants étaient aussi examinées dans les analyses sus-jacentes. Les covariables comme l’âge, le sexe, le niveau d’études, le statut marital, et le QI prémorbide étaient inclus dans le modèle multivarié. De plus, les données de chaque point de temps de suivi étaient retirées de la ligne de base pour que chaque participant examine la magnitude du changement dans le temps. Des analyses de mesures ANCOVA répétées étaient appliquées pour évaluer le changement de la ligne de base de la même façon que celle décrite plus haut.
Enfin, des analyses post-hoc examinaient l’impact du génotype APOE sur la fonction cognitive en relation avec l’intervention, aussi bien que l’impact de l’intervention pour les participants avec de légers troubles cognitifs.
Tous les tests statistiques de signification étaient bilatéraux, et  = 0.05 était considéré comme statistiquement significatif. = 0.05 était considéré comme statistiquement significatif.
RESULTATS
Trois cent onze individus ont été examinés pour admissibilité par appel téléphonique. Le SCHEMA indique le flux de participants depuis le moment de la sélection jusqu’à la fin de l’étude à 18 mois. Cent soixante-dix adultes âgés répondaient aux critères et ont consenti à prendre part à l’essai, parmi lesquels 59 avaient un domaine simple de déficit mnésique isolé ; 28, un domaine multiple de déficit mnésique isolé ; et 15, un déficit non mnésique.3 Le TABLEAU 1 montre leurs caractéristiques démographique et clinique.
|
|

|
Figure. Distribution des participants de la sélection à la fin de l’évaluation finale du suivi
Le nombre de cas complets peut varier selon le point final(to the end point) à cause de données manquantes
|
|
|
|
|

|
|
Tableau 1. Caractéristiques de ligne de base des participants à l’essai
|
|
|
Effet de l’Intervention sur la Fonction Cognitive, l’Humeur, et la Qualité de Vie
Le TABLEAU 2 montre les changements en intention de traiter dans les scores cognitifs, l’humeur, et la qualité de vie pendant 18 mois par groupe. A la fin de l’étude, les participants du groupe d’exercice avaient de meilleurs scores ADAS-Cog que ceux du groupe-contrôle de soin habituel (P = .04). Les participants du groupe d’activité physique avaient aussi de meilleurs rappels différés que ceux du groupe de soin habituel. Lorsque les analyses étaient limitées aux participants avec un déficit cognitif léger (TABLEAU 3 ; analyse post hoc), seuls les scores ADAS-Cog étaient significativement différents. L’analyse de cas complets a confirmé que les participants randomisés pour le groupe d’exercice avait de meilleurs scores ADAS-Cog que ceux du groupe-contrôle de soin habituel pendant tout l’essai (TABLEAU 4). Ils avaient aussi des rappels différés significativement meilleurs et des scores de l’Echelle CDR (Clinical Dementia Rating sum of boxes) qui tient compte à la fois des déficits cognitifs et des activités de la vie quotidienne, inférieurs à ceux du groupe-contrôle de soin habituel (TABLEAU 4).
|
|

|
|
Tableau 2. Effets de l’intervention et du temps sur les résultats cognitifs, l’humeur, et la qualité de vie des participants (Méthode en intention de traiter en utilisant des données imputées multiples)a
|
|
|
|
|

|
|
Tableau 3. Effets de l’intervention et du temps sur les résultats cognitifs, l’humeur, et la qualité de vie des participants avec un déficit cognitif léger seulement (méthode en intention de traiter utilisant les données imputées)a
|
|
|
|
|

|
|
Tableau 4. Effets de l’intervention et du temps sur les résultats cognitifs, l’humeur, et la qualité de vie des participants qui ont terminé toutes les évaluations (analyse de cas complet)a
|
|
|
Le TABLEAU 5 montre des changements de mesures d’activité physique tout au long de l’essai selon l’appartenance au groupe. Comme attendu, les participants du groupe d’activité physique ont augmenté leur niveau d’activité physique en comparaison avec les contrôles de soin habituel. A 6 mois, les participants du groupe d’activité physique faisaient environ 9000 pas par semaine de plus que le groupe-contrôle de soin habituel du fait à la fois d’une augmentation des pas dans le groupe et d’une diminution dans le groupe-contrôle. Cette différence entre les groupes, respectivement, est restée relativement stable à 12 mois, mais a baissé à approximativement 6000 pas par semaine à 18 mois. Il y avait une tendance non significative pour les participants du groupe d’activité physique à passer plus de temps dans des activités modérées et plus que les contrôles de soin habituel. L’adhésion à l’activité physique pour les 24 semaines était de 78,2%. Nous avons aussi examiné la proportion de personnes dans chaque groupe qui a atteint l’équivalent de 70 000 pas ou plus par semaine à chaque point de temps (analyse de cas complet seulement). A 6 mois, 22 des 85 participants (25,0%) dans l’activité physique et 15 des 85 participants (17,6%) dans les groupes-contrôle de soin habituel ont atteint le nombre cible de pas ( 21= 1,69 ; P = .19). A 12 mois 25 des 85 (29,4%) du groupe d’activité physique et 15 des 85 (17,6%) des groupes de soin habituel ont atteint la cible ( 21= 1,69 ; P = .19). A 12 mois 25 des 85 (29,4%) du groupe d’activité physique et 15 des 85 (17,6%) des groupes de soin habituel ont atteint la cible ( 21= 3,27 ; P = .07), et à 18 mois la proportion atteignant le nombre-cible de pas était de 16 sur 85 (18,8%) pour les deux groupes ( 21= 3,27 ; P = .07), et à 18 mois la proportion atteignant le nombre-cible de pas était de 16 sur 85 (18,8%) pour les deux groupes ( 21= 0 ; P >.99). 21= 0 ; P >.99).
|
|

|
|
Tableau 5. Effets de l’intervention sur les mesures objectives d’activité physique en relation avec la ligne de base (analyse en intention de traiter utilisant les données d’imputation multiple)a
|
|
|
Des événements défavorables étaient définis comme n’importe quel symptôme physique ou psychologique survenu à n’importe quel moment après la randomisation et qui conduisait à l’exclusion du participant de toute participation ultérieure ou qui obligeait le participant à interrompre l’étude temporairement. Dix événements se sont produits pendant l’étude et le personnel d’intervention jugea qu’il était improbable qu’un seul de ces événements fût causé directement par l’intervention (TABLEAU 6).
|
|

|
|
Tableau 6. Evénements indésirables et discontinuité de l’intervention pendant la période active (24 premières semaines) ou après la période active (de 24 semaines à 18 mois)
|
|
|
Nous avons mené une série d’analyses post hoc pour déterminer si les différences observées entre l’activité physique et les groupes-contrôle de soin habituel pouvaient être expliquées par des pertes différentielles de suivi. Les femmes étaient plus enclines à abandonner dans les deux groupes, et ceux qui abandonnaient avaient des scores ADAS-Cog plus élevés que ceux qui restaient dans l’essai (TABLEAU 7).
|
|

|
|
Tableau 7. Caractéristiques démographiques et cliniques des participants de ligne de base qui ont terminé et abandonné l’essaia
|
|
|
Nous avons aussi terminé une série d’analyses post hoc pour clarifier le fait de savoir si la réponse au traitement était associée au génotype APOE. Cinquante et un participants à l’étude (30%) étaient porteurs d’1 allèle APOE  4 (24 dans le groupe d’activité physique et 27 dans le groupe-contrôle de soin habituel). Dans l’analyse de cas complet de 18 mois, il y avait un effet différentiel de l’exercice sur les scores ADAS-Cog selon le statut porteur de l’APOE 4 (24 dans le groupe d’activité physique et 27 dans le groupe-contrôle de soin habituel). Dans l’analyse de cas complet de 18 mois, il y avait un effet différentiel de l’exercice sur les scores ADAS-Cog selon le statut porteur de l’APOE  4, avec le changement des scores ADAS-Cog au long du déroulement de l’étude pour les non porteurs de l’APOE 4, avec le changement des scores ADAS-Cog au long du déroulement de l’étude pour les non porteurs de l’APOE  4 dans le groupe d’activité physique étant significativement meilleur que les scores des sujets dans l’autre groupe combiné (F1=8,73 ; P=.004). Les scores ADAS-Cog parmi les non porteurs APOE 4 dans le groupe d’activité physique étant significativement meilleur que les scores des sujets dans l’autre groupe combiné (F1=8,73 ; P=.004). Les scores ADAS-Cog parmi les non porteurs APOE  4 dans le groupe d’activité physique étaient différents des porteurs APOE 4 dans le groupe d’activité physique étaient différents des porteurs APOE  4 et des non porteurs du groupe-contrôle de soin habituel (F1=4,59 ; P=.04 et F1=5,01I ; P=.03, respectivement).Il n’y a eu aucune autre différence significative intra-participant. 4 et des non porteurs du groupe-contrôle de soin habituel (F1=4,59 ; P=.04 et F1=5,01I ; P=.03, respectivement).Il n’y a eu aucune autre différence significative intra-participant.
COMMENTAIRE
A notre connaissance, cet essai est le premier à démontrer que l’exercice améliore la fonction cognitive chez l’adulte âgé victime de déficit cognitif léger subjectif et objectif. Les bénéfices de l’activité physique étaient apparents après 6 mois et persistaient pendant au moins 12 mois après l’arrêt de l’intervention. L’amélioration moyenne de 0,69 points dans le score ADAS-Cog comparé au groupe de contrôle de soin habituel à 18 mois est petite mais potentiellement importante lorsque l’on considère l’activité physique relativement modeste entreprise par les participants de l’étude.
L’intervention de l’étude a résulté en 142 minutes d’activité physique en plus par semaine ou 20 minutes par jour que le soin habituel. A la différence des médicaments, dont on a trouvé qu’ils n’avaient pas d’effet significatif sur les troubles cognitifs légers à 36 mois, 39l’activité physique avait l’avantage de bénéfices dans le domaine de la santé qui ne sont pas limités à la fonction cognitive seule, comme le laissaient penser les découvertes sur la dépression, 40la qualité de vie,41 les chutes,42 la fonction cardiovasculaire,43 et le handicap.44
Dans notre étude, les participants du groupe d’intervention ont eu une amélioration de 1,3 point dans ADAS-Cog quant au groupe-contrôle de soin habituel après 6 mois. Ce résultat se compare favorablement avec l’amélioration rapportée de 0,5 points associée à l’utilisation de donepezil.4 De façon importante, les effets bénéfiques de l’activité physique étaient supportés, bien qu’atténués, pendant les 18 mois de la période de suivi (différence moyenne de 0,69 points sur ADAS-Cog) vs la différence non significative de 0,2 points associée avec l’utilisation de donepezil à 18 mois.4 De façon importante, les résultats ADAS-Cog restèrent largement inchangés lorsque seules les personnes répondant aux critères pour le diagnostic de troubles cognitifs légers étaient incluses dans les analyses, laissant penser que notre stratégie d’échantillonnage ne peut expliquer nos découvertes (n’étaient pas dus à l’inclusion de personnes avec des plaintes de mémoire subjectives mais sans troubles cognitifs objectifs).
Les mécanismes par lesquels l’activité physique améliore la cognition chez la personne âgée à risque élevé de démence ne sont pas clairs. Un des mécanismes possible est une altération du fonctionnement vasculaire cérébral et l’irrigation du cerveau. Des études impliquant des modèles animaux ont montré que l’activité physique peut stimuler l’angiogénèse, l’irrigation du cerveau et l’intégrité neuro-vasculaire en 3 à 4 semaines.45 Un autre mécanisme possible est un enrichissement environnemental lié à une plus grande activité physique. 46 Une recherche de base a montré que des environnements riches stimulent l’activité46, 47et contribuent à augmenter la plasticité du cerveau par la synaptogénèse, la neurogénèse, et l’atténuation de la réponse neurale au stress. 48,49 Uda et al49 par exemple ont comparé l’hippocampe de rats de contrôle adultes avec des rats qui couraient sur un tapis de jogging 30 minutes par jour pendant 7 jours. Les rats actifs avaient plus d’astrocytes et de neuroblastes avec une capacité proliférative dans la zone sous-granulaire du gyrus dentelé de l’hippocampe, aussi bien qu’un nombre élevé de neurones au stade de division que les rats de contrôle. Les auteurs ont spéculé que les changements observés étaient liés à une production accrue de facteur 2 de croissance de fibroblastes chez le rat actif. De même, Kronenberg et al48ont démontré dans un modèle souris que courir dans une roue induisait une neurogénèse chez l’animal âgé. Ils ont suggéré que cet effet était partiellement dû aux récepteurs N-méthyl-D-asparte, glissement de l’expression du récepteur corticoïde dans l’hippocampe, et l’activation du facteur de croissance insuline-like IGF1, le facteur de croissance vasculaire endothélial, le facteur neurotrophique dérivé du cerveau, et les endorphines.
Chez l’humain, Colcombe et al50ont démontré que l’activité physique est liée à une irrigation sanguine élevée des régions de cerveau qui modulent l’attention. Vingt-neuf adultes âgés très actifs ont été assignés aléatoirement à soit une activité d’aérobic ou d’étirement soit à une activité tonifiante. Le but du groupe d’exercice d’aérobic était d’améliorer l’aptitude cardiorespiratoire, alors que le groupe d’étirement et de tonification servait de groupe-contrôle. Les participants des deux groupes se rencontraient 3 fois par semaine pendant 40 à 45 minutes. Après 6 mois, les participants du groupe aérobic montraient une activité significativement plus importante liée à des tâches dans les zones de contrôle de l’attention, comme le gyrus frontal médian, le gyrus frontal supérieur, et le lobule pariétal supérieur.50 Les auteurs ont suggéré que l’activité augmentée était due à la synaptogénèse de l’activité physique stimulée, un apport sanguin accru, et des effets cholinergiques non spécifiés.
Une preuve clinique suggère que l’activité physique augmente le bien-être, comme il a été démontré dans une méta-analyse sur 36 études d’activité physique chez des adultes âgés. 40 Les résultats de notre essai n’ont pas réussi à montrer un effet significatif de l’activité physique sur l’humeur ou la qualité de vie, ce qui suggère qu’il est improbable qu’un bien-être amélioré ait confondu nos résultats.
L’interaction observée entre activité physique et génotype APOE  4 présente un intérêt, bien que post hoc. Les porteurs APOE 4 présente un intérêt, bien que post hoc. Les porteurs APOE  4 montrent des changements métaboliques et structurels dans les zones du cerveau connues pour être affectées chez les personnes avec une MA bien avant le développement de troubles cognitifs cliniquement manifestes. 51Par conséquent, il est possible que les bénéfices cognitifs liés à l’activité physique dans cet essai aient été atténués par des effets de APOE 4 montrent des changements métaboliques et structurels dans les zones du cerveau connues pour être affectées chez les personnes avec une MA bien avant le développement de troubles cognitifs cliniquement manifestes. 51Par conséquent, il est possible que les bénéfices cognitifs liés à l’activité physique dans cet essai aient été atténués par des effets de APOE  4 délétères préexistants ou en train de se développer. 4 délétères préexistants ou en train de se développer.
Cet essai présente des limites. L’échantillon de l’étude était relativement jeune et pouvait ne pas représenter correctement la population à risque le plus élevé de déficit cognitif. De plus, il s’agissait d’un essai sur un seul site de volontaires motivés de la communauté qui étaient exempts de morbidités médicales significatives et de démence et, en conséquence, les résultats ne peuvent pas être aisément transmissibles à une population clinique. De plus, l’étude n’avait aucun accès à l’imagerie ou à la biochimie cérébrale, de sorte que les mécanismes physiologiques potentiels servant d’intermédiaire entre la relation entre l’activité physique et la fonction cognitive ne pouvaient être identifiés. La batterie neuropsychologique utilisée pour évaluer les participants était limitée à une mesure générale de fonction cognitive (ADAS-Cog), la mémoire verbale et l’aisance verbale, et la substitution de codage. En conséquence, nous n’avons pas été capables de déterminer si les compétences cognitives spécifiques sont plus susceptibles aux changements liés à une activité physique que d’autres. En outre, la taille de l’effet de l’intervention était petite et, alors qu’elle soutient le concept que l’activité physique peut réduire le taux de déclin cognitif, la signification clinique de nos découvertes reste à établir. Enfin, les résultats de cet essai ne peuvent être utilisés pour déduire que l’activité physique réduit le risque de démence parmi les adultes âgés à risque, parce que l’étude n’était pas faite pour examiner le développement de la démence.
Un des mérites importants de cet essai était de démontrer le bénéfice potentiel d’une simple intervention qui est presque universellement disponible. L’intervention était basée sur les étapes de modèle de changement que l’on a montré comme étant efficace dans l’augmentation et le maintien de l’activité physique chez l’adulte âgé. 37Les stratégies utilisées comprenaient des programmes individuels sur mesure, en donnant des réponses quant au progrès, et en augmentant les bénéfices perçus par les participants comme étant plus actifs physiquement. Le programme était sûr et montrait une bonne participation.
En résumé, les résultats de cet essai randomisé indiquent qu’un programme d’activité physique de 142 minutes additionnelles d’exercices par semaine en moyenne améliorait modestement la cognition liée aux contrôles chez l’adulte âgé ayant des troubles de mémoire subjectifs et objectifs.
Informations sur les auteurs
Correspondance : Nicola T. Lautenschlager, MD, Academic Unit for Psychiatry of Old Age, University of Melbourne, Normanby Unit, St Vincent’s Aged Psychiatry Service, St George’s Campus, St Vincent’s Hospital, 283 Cotham Rd, Kew, Victoria, 3101 Australia (nicolatl{at}unimelb.edu.au).
Affiliations des auteurs: WA Centre for Health and Ageing (Drs Lautenschlager, Cox, Flicker, Greenop, and Almeida); School of Psychiatry and Clinical Neurosciences (Drs Lautenschlager and Almeida), School of Medicine and Pharmacology (Drs Cox and Flicker), and School of Pathology and Laboratory Medicine (Dr van Bockxmeer), University of Western Australia, School of Exercise, Biomedical and Health Sciences, Edith Cowan University (Dr Foster), Neurosciences Unit (Dr Foster) and Epidemiology Branch (Dr Xiao), Department of Health Western Australia, Sir James McCusker Alzheimer’s Disease Research Unit, Hollywood Private Hospital (Dr Foster), and Royal Perth Hospital, Perth (Drs Lautenschlager, Flicker, van Bockxmeer, and Almeida) and Academic Unit for Psychiatry of Old Age, St Vincent’s Health, Department of Psychiatry, University of Melbourne, Melbourne (Dr Lautenschlager), Australia.
Contributions de l’auteur : Le Dr Lautenschlager a eu un accès complet à toutes les données de l’étude et accepte la responsabilité de l’intégrité des données et l’exactitude de l’analyse des données.
Concept et conception de l’étude : Lautenschalger, Cox, Flicker, Foster, Almeida.
Acquisition des données : Lautenschalger, Cox, Flicker, Greenop, van Bockxmeer, Almeida.
Analyse et interprétation des données : Lautenschalger, Cox, Flicker, Foster, van Bockxmeer, Xiao, Greenop, Almeida.
Rédaction du manuscrit : Lautenschalger, Cox, Flicker, Greenop, Almeida.
Révision critique du manuscrit : Lautenschalger, Cox, Flicker, Foster, van Bockxmeer, Xiao, Greenop, Almeida.
Analyse statistique : Lautenschalger, Flicker, Foster, van Bockxmeer, Xiao, Greenop, Almeida.
Financement obtenu : Lautenschalger, Cox, Flicker, Foster, Almeida.
Soutien administratif, technique, ou matériel : Lautenschalger, Cox, Flicker, Foster, van Bockxmeer, Greenop, Almeida.
Surveillance de l’étude : Lautenschalger, Cox, Flicker.
Liens financiers : Aucun déclaré.
Financement/Soutien : L’étude a été soutenue par la bourse 303172 du Conseil de Recherche National Médical et de Santé d’Australie (Drs Lautenschlager, Almeida, Flicker, Cox et Foster).
Rôle des Sponsors : Les sponsors ne jouaient aucun rôle dans la conception et la conduite de l’étude ; collecte, gestion, analyse, et interprétation des données ; ou préparation, examen, ou approbation du manuscript.
Contributions Supplémentaires : Nous remercions les participants FABS et le personnel de recherche.
Voir aussi p 1077 et la Page du Patient.
BIBLIOGRAPHIE
 |  |
1. Brookmeyer R, Johnson E, Ziegler-Graham K, Arrighi HM. Forecasting the global burden of Alzheimer’s disease. Alzheimers Dement. 2007;3:186-191.
2. Van Oijen M, de Long FJ, Hofman A, Koudstaal PJ, Breteler MMB. Subjective memory complaints, education, and risk of Alzheimer’s disease. Alzheimers Dement. 2007;3:92-97.
3. Petersen RC. Mild cognitive impairment as a diagnostic entity. J Intern Med. 2004;256(3):183-194.
PUBMED
4. Petersen RC, Thomas RG, Grundman M, et al.. Vitamin E and donepezil for the treatment of mild cognitive impairment. N Engl J Med. 2005;352(23):2379-2388.
PUBMED
5. Feldman HH, Ferris S, Winblad B, et al.. Effect of rivastigmine on delay to diagnosis of Alzheimer’s disease from mild cognitive impairment: the InDDEx study. Lancet Neurol. 2007;6(6):501-512.
PUBMED
6. Jelic V, Kivipelto M, Wilblad B.. Clinical trials in mild cognitive impairment: lessons for the future. J Neurol Neurosurg Psychiatry. 2006;77(4):429-438.
FREE FULL TEXT
7. Thal LJ, Ferris SH, Kirby L, et al.. A randomized, double-blind, study of Rofecoxib in patients with mild cognitive impairment. Neuropsychopharmacology. 2005;30(6):1204-1215.
PUBMED
8. Durga J, van Boxtel MPJ, Schouten EG, et al.. Effect of 3-year folic acid supplementation on cognitive function in older adults in the FACIT trial: a randomised, double-blind, controlled trial. Lancet. 2007;369(9557):208-216.
PUBMED
9. McMahon JA, Green TJ, Skeaff CM, et al.. A controlled trial of homocysteine lowering and cognitive performance. N Engl J Med. 2006;354(26):2764-2772.
PUBMED
10. Heart Protection Study Collaborative Group. MRC/BRF Heart Protection Study of cholesterol loweringwith simvastatin in 20 536 high-risk individuals: a randomised placebo-controlled trial. Lancet. 2002;360(9326):7-22.
PUBMED
11. Forette F, Seux M, Staessen JA, et al.. The prevention of dementia with antihypertensive treatment: new evidence from the Systolic Hypertension in Europe (Syst-Eur) Study. Arch Intern Med. 2002;162(18):2046-2052.
FREE FULL TEXT
12. Lithell H, Hansson L, Skoog I, et al.. The Study of Cognition and Prognosis in the Elderly (SCOPE): principle results of a randomized double-blind intervention trial. J Hypertens. 2003;21(5):875-886.
PUBMED
13. Weuve J, Kang JH, Manson JE, Breteler MMB, Ware JH, Grodstein F. Physical activity, including walking, and cognitive function in older women. JAMA. 2004;292(12):1454-1461.
FREE FULL TEXT
14. Abbott RD, White LR, Ross GW, Masaki KH, Curb JD, Petrovitch H. Walking and dementia in physically capable elderly men. JAMA. 2004;292(12):1447-1453.
FREE FULL TEXT
15. Larson EB, Wang L, Bowen JD, et al.. Exercise is associated with reduced risk for incident dementia among persons 65 years of age and older. Ann Intern Med. 2006;144(2):73-81.
FREE FULL TEXT
16. Podewils LJ, Guallar E, Kuller LH, et al.. Physical activity, APOE genotype, and dementia risk: findings from the Cardiovascular Health Cognition Study. Am J Epidemiol. 2005;161:639-651.
FREE FULL TEXT
17. van Gelder BM, Tijhuis MAR, Kalmijn S, Giampaoli S, Nissinen A, Kromhout D. Physical activity in relation to cognitive decline in elderly men: the FINE Study. Neurology. 2004;63(12):2316-2321.
FREE FULL TEXT
18. Lines CR, McCarroll KA, Lipton RB, Block GA.; Prevention of Alzheimer’s In Society’s Elderly Group. Telephone screening for amnestic mild cognitive impairment. Neurology. 2003;60(2):261-266.
FREE FULL TEXT
19. Almeida OP, Almeida SA. Short versions of the geriatric depression scale: a study of their validity for the diagnosis of a major depressive episode according to ICD-10 and DSM-IV. Int J Geriatr Psychiatry. 1999;14(10):858-865.
PUBMED
20. Folstein MF, Folstein SE, McHugh PR. "Minimental state": a practical method for grading the cognitive state of patients for the clinician. J Psychiatr Res. 1975;12(3):189-198.
PUBMED
21. Morris J.. The Clinical Dementia Rating (CDR): current version and scoring rules. Neurology. 1993; 43(11):2412-2413.
FREE FULL TEXT
22. Welsh KA, Butters N, Mohs RC, et al.. The Consortium to Establish a Registry for Alzheimer’s Disease (CERAD), V: a normative study of the neuropsychological battery. Neurology. 1994;44(4):609-614.
FREE FULL TEXT
23. World Health Organization. International Statistical Classification ofDiseases, 10th Revision (ICD-10). Geneva, Switzerland: World Health Organization; 1992.24. CERAD. Consortium to Establish a Registry for Alzheimer’s Disease: Documentation and Data Archive Revision 2.0 [CD-ROM]. Durham, NC: Duke University Medical Centre;1996;revision 2.0.25. Stewart AL, Mills KM, King AC, Haskell WL, Gillis D, Ritter PL. CHAMPS physical activity questionnaire for older adults: outcomes for interventions. Med Sci Sports Exerc. 2001;33:1126-1141.
PUBMED
26. Tudor-Locke C, Williams JE, Reis JP, Pluto D. Utility of pedometers for assessing physical activity: convergent validity. Sports Med. 2002;32(12):795-808.
PUBMED
27. Miller R, Brown W, Tudor-Locke C.. But what about swimming and cycling? how to "count" nonambulatory activity when using pedometers to assess physical activity. J Phys Act Health. 2006;3(3):257-266.
28. Tudor-Locke C, Bassett DR. How many steps are enough? preliminary pedometer indices for public health. Sports Med. 2004;34(1):1-8.
PUBMED
29. Rosen WG, Mohs RC, Davis KL. A new rating scale for Alzheimer’s Disease. Am J Psychiatry. 1984;141(11):1356-1364.
FREE FULL TEXT
30. Wechsler D.. The Wechsler Adult Intelligence Scale—Third Edition—Austrailian Language Adaptation (WAIS-III). San Antonio, TX: The Psychological Corp; 1997.31. Delis DE, Kaplan E, Kramer J. The Delis-Kaplan Executive Function System. 2nd ed. San Antonio, TX: The Psychological Corp; 2001.32. Beardsall L.. Development of the Cambridge Contextual Reading Test for improving the estimation of premorbid verbal intelligence in older persons with dementia. Br J Clin Psychol. 1998;37(pt 2):229-240.
PUBMED
33. Beck AT, Ward CH, Mendelson M, Mock J, Erbaugh J. An inventory for measuring depression. Arch Gen Psychiatry. 1961;4:561-571.
FREE FULL TEXT
34. Ware JE Jr, Gandek B. Overview of the SF-36 Heath Survey and the International Quality of Life Assessment (IQOLA) project. J Clin Epidemiol. 1998;51(11):903-912.
PUBMED
35. Hixson JE, Vernier DT. Restriction isotyping of human apolipoprotein E by gene amplification and cleavage with HhaI. J Lipid Res. 1990;31(3):545-548.
ABSTRACT
36. Pate RR, Pratt M, Blair SN, et al.. Physical activity and public health: a recommendation from the Centers for Disease Control and Prevention and the American College of Sports Medicine. JAMA. 1995;273(5):402-407.
FREE FULL TEXT
37. Cox KL, Burke V, Gorely TJ, Beilin LJ, Puddey IB. Controlled comparison of retention and adherence in home- vs center-initiated exercise interventions in women ages 40-65 years: the S.W.E.A.T. Study. Prev Med. 2003;36(1):17-29.
PUBMED
38. Birks J.. Cholinesterase inhibitors for Alzheimer’s disease. Cochrane Database Syst Rev. 2006;(1):CD005593.39. Birks J, Flicker L.. Donepezil for mild cognitive impairment. Cochrane Database Syst Rev. 2006;(3):CD006104.40. Netz Y, Wu M-J, Becker BJ, Tenenbaum G. Physical activity and psychological well-being in advanced age: a meta-analysis of intervention studies. Psychol Aging. 2005;20(2):272-284.
PUBMED
41. Spirduso WW, Cronin DL. Exercise doseresponse effects on quality of life and independent living in older adults. Med Sci Sports Exerc. 2001;33(6)(suppl):S598-S608.
PUBMED
42. Chang JT, Morton SC, Rubenstein LZ, et al.. Interventions for the prevention of falls in older adults: systematic review and meta-analysis of randomised clinical trials. BMJ. 2004;328(7441):680-686.
FREE FULL TEXT
43. Thompson PD, Buchner D, Pina IL, et al.. Exercise and physical activity in the prevention and treatment of atherosclerotic cardiovascular disease. Circulation. 2003;107(24):3109-3116.
FREE FULL TEXT
44. Keysor JJ. Does late-life physical activity or exercise prevent or minimize disablement?AmJ Prev Med. 2003;25(3)(suppl 2):129-136.
45. Swain RA, Harris AB, Wiener EC, et al.. Prolonged exercise induces angiogenesis and increases cerebral blood flow volume in primary motor cortex of the rat. Neuroscience. 2003;117(4):1037-1046.
PUBMED
46. van Praag H, Kempermann G, Gage FH. Neural consequence of environmental enrichment. Nat Rev Neurosci. 2000;1(3):191-198.
PUBMED
47. Stranahan AM, Khalil D, Gould E. Social isolation delays the positive effect of running on adult neurogenesis. Nat Neurosci. 2006;9(4):526-533.
PUBMED
48. Kronenberg G, Bick-Sander A, Bunk E, et al.. Physical exercise prevents age-related decline in precursor cell activity in the mouse dentate gyrus. Neurobiol Aging. 2006;27(10):1505-1513.
PUBMED
49. Uda M, Ishido M, Kami K, Musuhara M.. Effects of chronic treadmill running on neurogenesis in the dentate gyrus of the hippocampus of adult rat. Brain Res. 2006;1104(4):64-72.
PUBMED
50. Colcombe SJ, Kramer AF, Erikson KI, et al.. Cardiovascular fitness, cortical plasticity, and aging. Proc Natl Acad Sci U S A. 2004;101(9):3316-3321.
FREE FULL TEXT
51. Bookheimer SY, Strojwas MH, Cohen MS, et al.. Patterns of brain activation in people at risk for Alzheimer’s disease. N Engl J Med. 2000;343(7):450-456.
PUBMED
ARTICLES EN RAPPORT
Activité physique des adultes âgés à risque de maladie d’Alzheimer
Eric B. Larson
JAMA. 2008;300:1077-1079.
Texte Complet
La condition physique des sujets âgés
Erin Brender, Alison E. Burke, et Richard M. Glass
JAMA. 2008;300:1104.
Texte Complet
Cette semaine dans le JAMA-Français
JAMA. 2008;300:995.
Texte Complet
|